Будущее – сегодня: что, если бы врачи могли анализировать состояние здоровья пациентов и планировать методы лечения и операции, используя ту же передовую технологию моделирования, которую используют автомобильная, аэрокосмическая, энергетическая промышленности?
Компьютерная биомеханика - актуальное, но ещё не до конца изведанное направление в науке. Именно поэтому разработчики и инженеры команды FlowVision не могут оставаться в стороне.
Технологии, дающие возможности
Задачи биомеханики - это не только подробная геометрическая модель, которая постоянно изменяет своё положение естественным образом, но и невероятная точность задания входных параметров. Какие технологии дают возможность моделировать изменения в человеческом теле?
Взаимодействие "жидкость - конструкция" (FSI)
FSI позволяет моделировать сопряжённые задачи взаимодействия внутреннего или внешнего потока жидкости с деформируемым телом. Это осуществляется с помощью интегрированного взамодействия FlowVision с КЭ-комплексами: SIMULIA Abaqus, MSC Nastran, АПМ WinMachine и другими. Например, В SIMULIA Abaqus моделируются деформации, а движение жидкости полностью моделируется во FlowVision.
Примеры ПО, с которым можно настроить связку
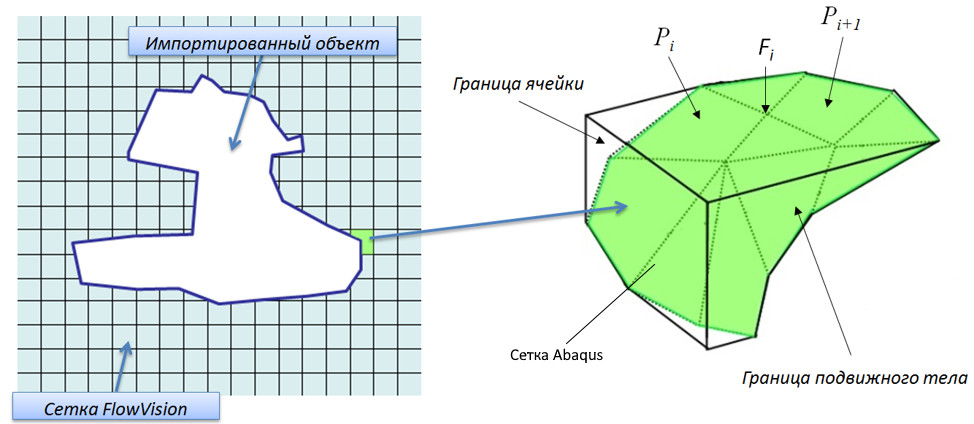
В интерфейсе FlowVision реализована возможность стыковки различных типов сеток и разных типов аппроксимаций, чтобы обеспечить двустороннюю передачу данных между КЭ-комплексом (например, Abaqus) и аэрогидродинамическим комплексом FlowVision.
Модификатор "Подвижное тело"
Эта технология позволяет задавать произвольный закон движения подвижного тела в пространстве с учётом влияния аэрогидродинамических и инерционных сил, а также контактное взаимодействие.
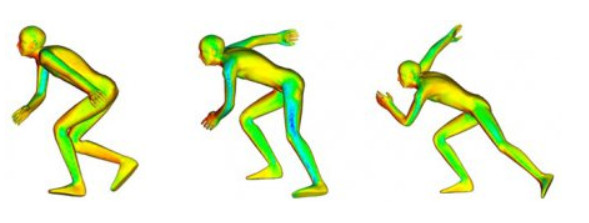
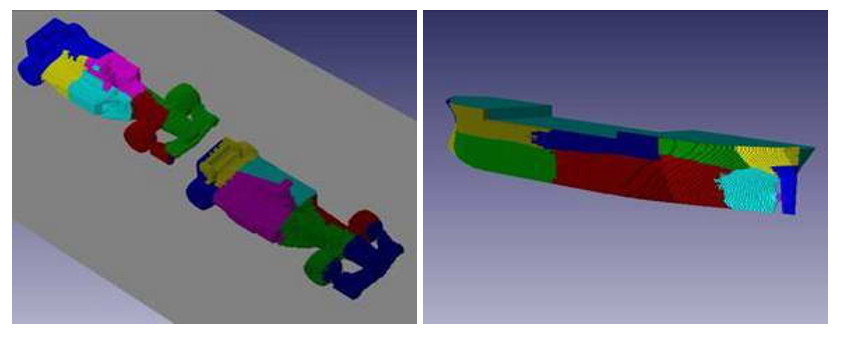
Пример применения модификатора "Подвижное тело" для моделирования движения спортсмена
Движение может быть задано для каждой из 6 степеней свобод как закон изменения поступательной и/или угловой скоростей и/или через силы и моменты.
Использование вывернутой геометрии позволяет рассчитывать внутренние полости органов, а для экономии времени расчёта для задач с заранее определённым законом движения (полученным, например, со сканеров и томографов) можно применять автоматическую замену геометрии в процессе расчёта.
Построение сетки для сложных геометрических моделей
Расчетная сетка FlowVision – структурированная, декартова, локально адаптивная. Локальная динамическая адаптация начальной сетки производится в соответствии с заданными пользователем критериями: возможна адаптация на границе, в области, по решению и градиенту.
Реализовано подсеточное разрешение геометрии и пристеночное призматическое разрешение пограничного слоя. Упрощения приграничных ячеек не производится.
Генерация сетки полностью автоматизирована. При применении модификатора "Подвижное тело", расчётная сетка автоматически перестраивается при обновлении положения Подвижного тела.
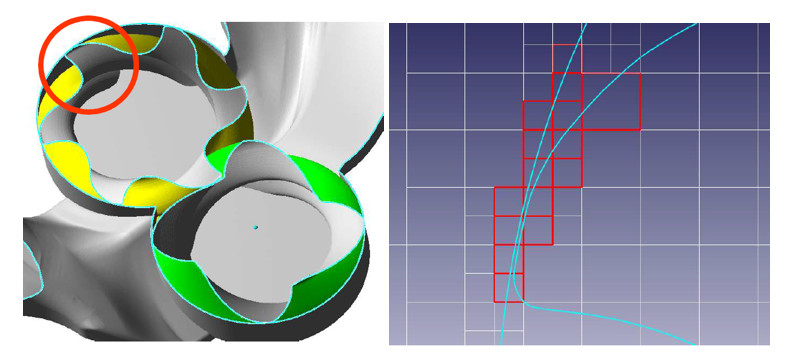
Взаимодействие сеток при совместном расчете
Модель зазора
Модель зазора – специальный метод моделирования физических процессов в узких каналах. Её использование позволяет не разрешать сеткой узкие каналы между поверхностями - автоматически включаются "зазорные" ячейки. В этом случае силы и диффузионные потоки в каналах рассчитываются по аналитическим выражениям.
Параллельные вычисления
При параллельных вычислениях расчётная сетка разбивается на несколько частей. Расчёт проводится для каждой части сетки отдельной копией решателя. Далее происходит обмен полученными данными между распараллеленными процессами.
FlowVision работает на компьютерах, имеющих смешанную архитектуру, совмещая межузловое MPI-распараллеливание с распараллеливанием по потокам в узле. Это позволяет добиться высококачественного масштабирования программного комплекса при работе на большом числе процессоров. То есть применять оптимальный по скорости обмена данными метод расчёта.
"Живое сердце" | Living Human Heart Project
Проект «Живое сердце» объединяет ведущих ученых, врачей , разработчиков и инженеров для проектирования и валидации высокоточных персонализированных цифровых моделей сердца человека.
В рамках проекта создается математическая модель работающего сердца, учитывающая электромеханические свойства мышечной ткани, работу предсердий, желудочков и клапанов (в том числе искусственных). Реалистичная симуляция кровотока в бьющемся человеческом сердце реализуется с помощью FSI технологии, учитывающей взаимодействия жидкость-конструкция между кровью и тканями сердца.
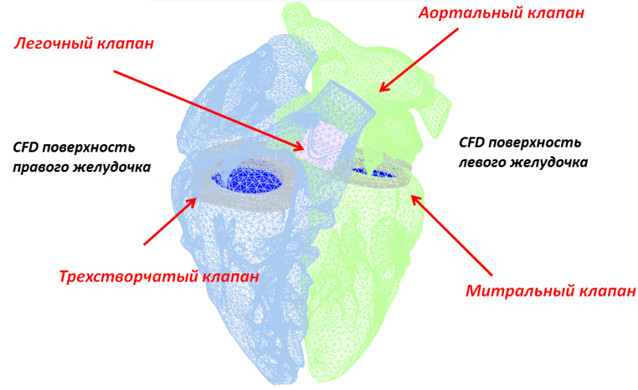
Модель SIMULIA «Живое сердце» – это высокоточная динамическая модель здорового четырехкамерного сердца взрослого мужчины. Она включает в себя анатомические составляющие сердца, такие как митральный, аортальный легочный и трехстворчатый клапаны, а также проксимальную сосудистую сеть: дугу аорты, легочную артерию и верхнюю полую вену.
Модель "Живое сердце"
Движение сердца регулируется реалистичной физикой электрических и структурных процессов, а также течением жидкости (крови).
Модель может использоваться для изучения как совместного электро-механического поведения сердца, в котором механический отклик обусловлен электрическим возбуждением, так и для изучения электрических импульсов сердца отдельно.
В результате исследований для модели сердца можно провести связанный электромеханический анализ цикла ударов с длительностью в одну секунду. Такая постановка соответствует стандартной частоте сердечных сокращений взрослого человека в расслабленном состоянии – 60 ударов в минуту.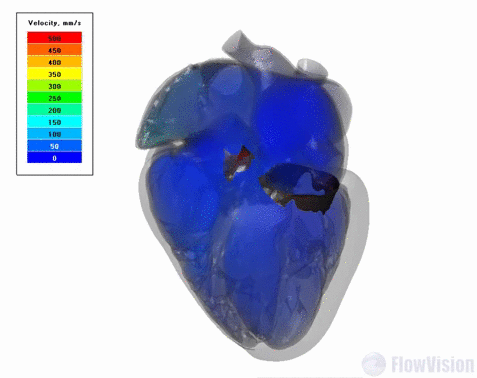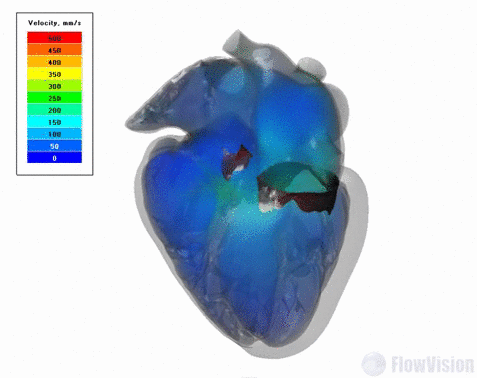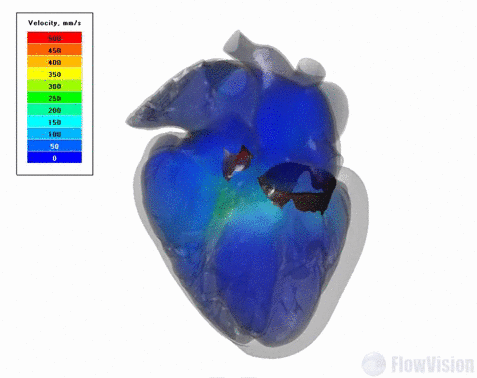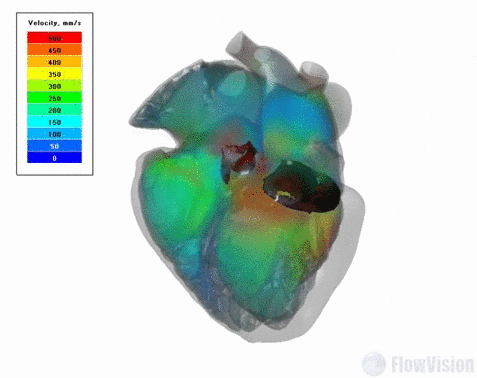
Результаты для модели сердца с натуральными клапанами: объемные скорости в сердце
Несмотря на то, что модель представляет собой здоровое сердце, на ней можно изучать аномальные состояния - болезни сердца. Такой эффект достигается при изменении геометрии составляющих сердца, свойств тканей и нагрузок. Кроме того, можно подключать к модели дополнительные составляющие (например, медицинские приборы), чтобы изучать их влияние на работу сердца и исследовать варианты лечения.
Участники проекта
Dassault Systemes; CAPVIDIA; TeSIS; Stony Brook University; Institute of Applied Mechanics, RWTH Aachen; Charité – Universitätsmedizin Berlin; University of California, San Francisco; Boston Scientific Corporation, Massachusetts Institute of Technology, National Institute of Cardiology, National Heart Centre Singapore, The German Heart Competence Center at Tübingen и другие.
Моделирование стента для аортального клапана
при сотрудничестве с Stony Brook University
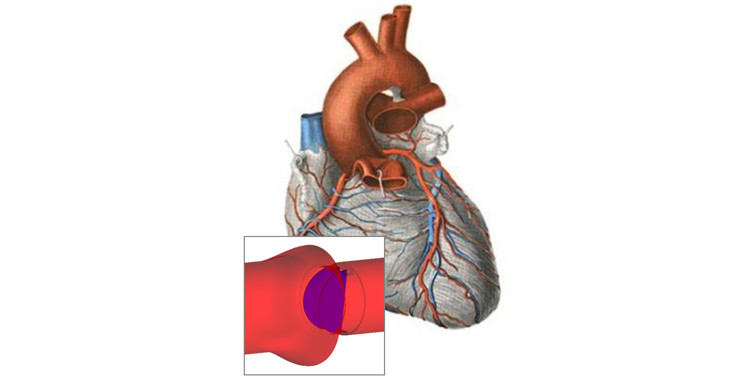
Стент представляет собой металлическую или пластиковую трубку, вставленную в просвет анатомического сосуда или канала для поддержания прохода открытым.
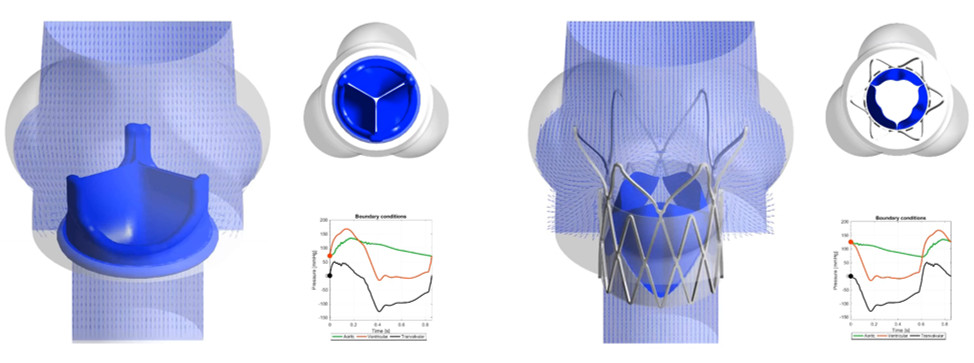
Модель стента (Courtesy of Stony Brook University)
Целью проекта является моделирование и оптимизация работы стента для аортального клапана. Это необходимо для увеличения продолжительности использования стента в реальном сердце.
Процесс моделирования разделен на два этапа:
1. Моделирование жидкостно-структурного взаимодействия (FSI) аортального канала, работающего без стента;
2. Введение стента и моделирование работы стента в канале аорты.
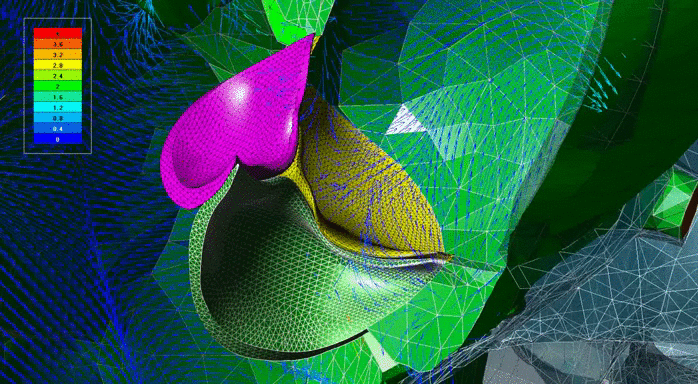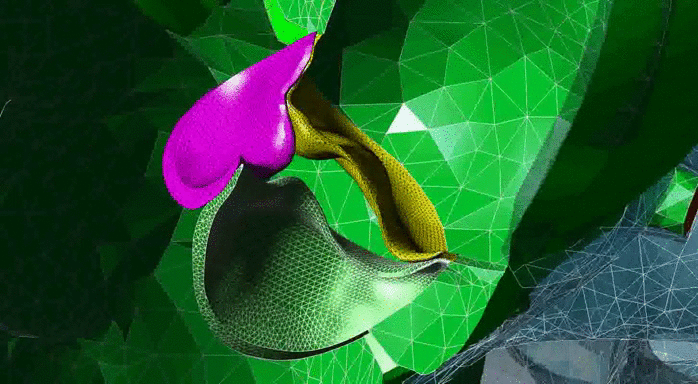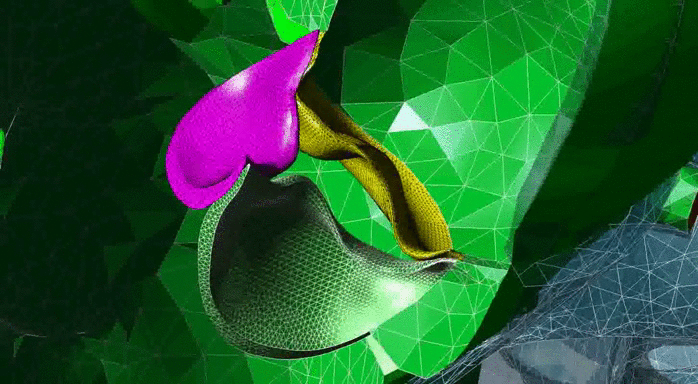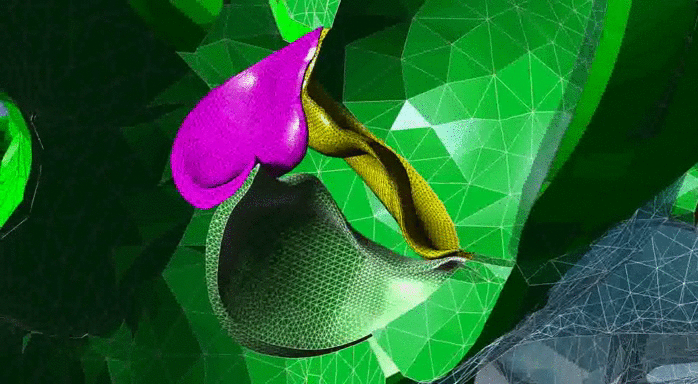
Результаты моделирования движения клапана под действием жидкости
Моделирование течения крови через митральный клапан
Механический митральный клапан был смоделирован в виде двух движущихся деталей, вращающихся вокруг своей оси под действием гидродинамических сил.
Задача решалась с помощью совместного расчёта: в Abaqus проводилось моделирование клапана и его деформация, а во FlowVision считалась гемодинамика крови.
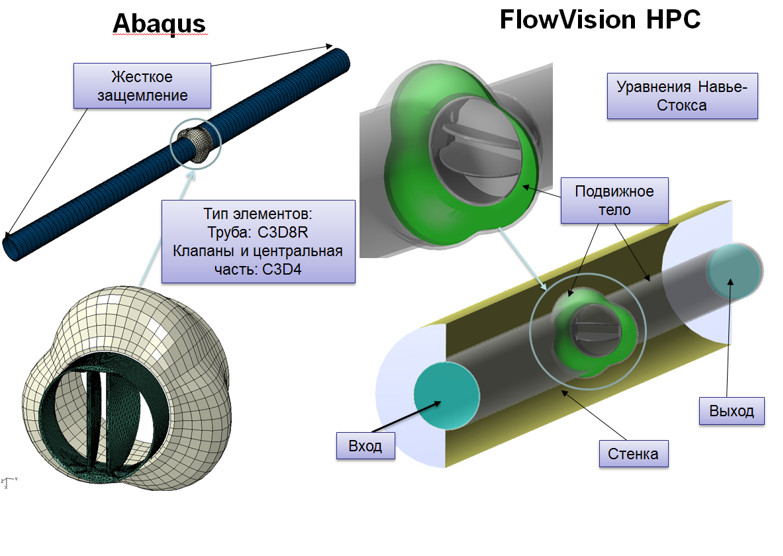
моделирование Митральной регургитация клапана
Митральная регургитация клапана возникает, если створки клапана перестают смыкаться, пропуская часть крови обратно в предсердие.
Это может вызвать повышение давления и привести к сердечной недостаточности.
Постановка задачи моделирования митральной регургитации: 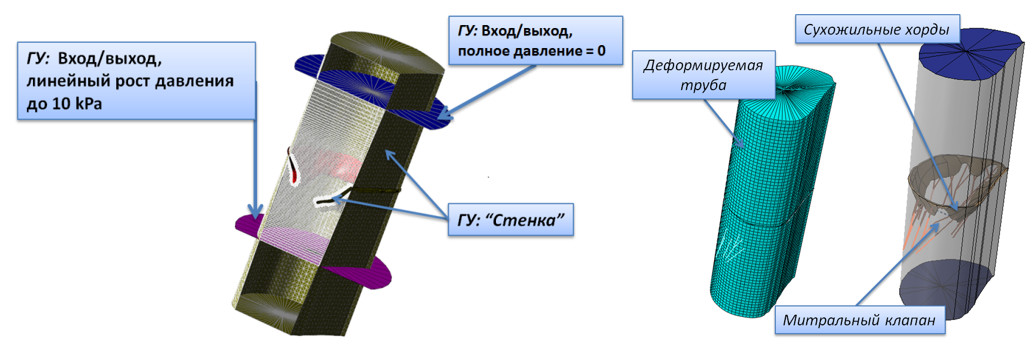
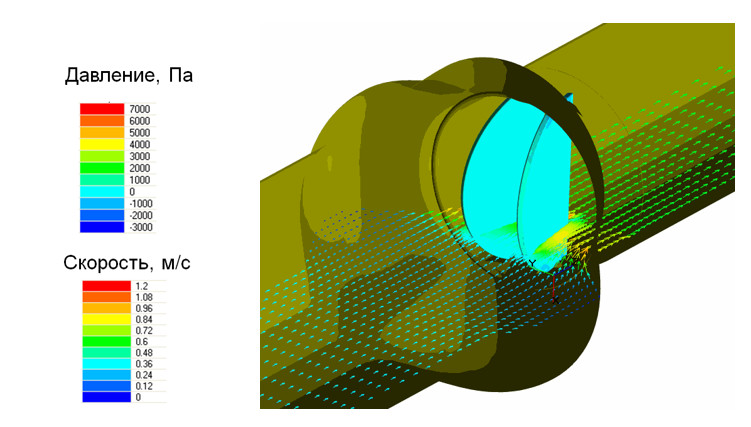
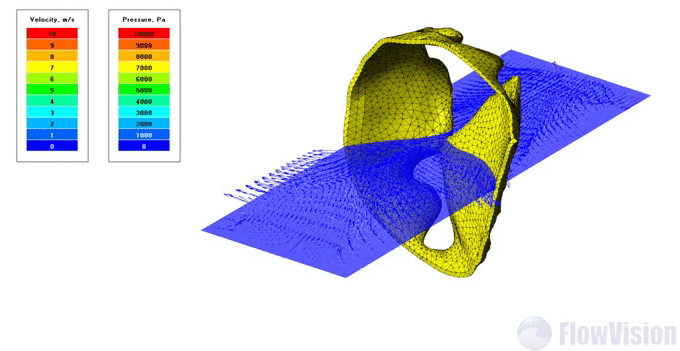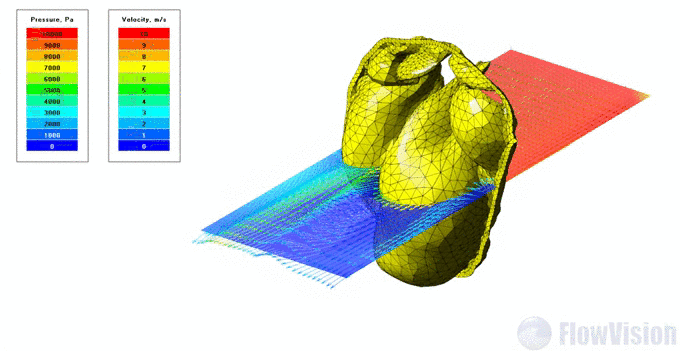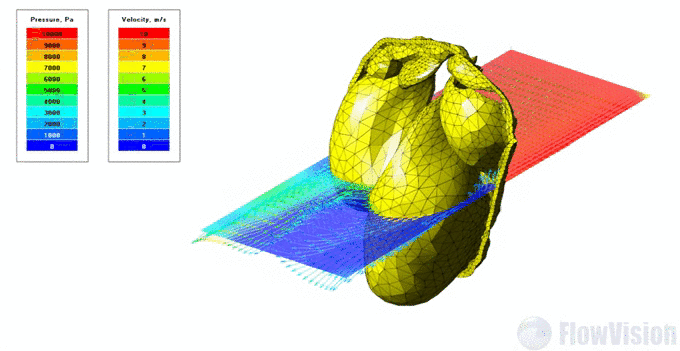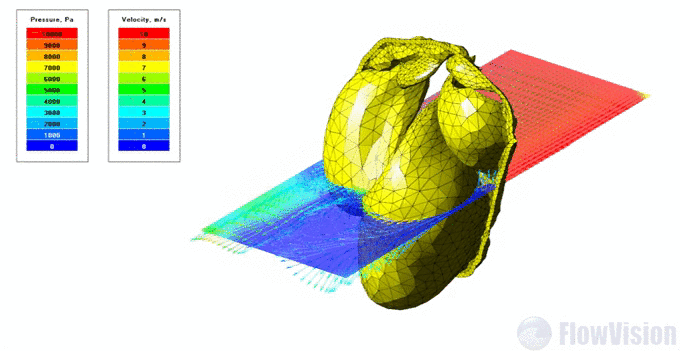 Результаты моделирования: распределение давления и скорости
Результаты моделирования: распределение давления и скорости
Моделирование течения крови через искусственный аортальный клапан
при сотрудничестве с RTWH Aachen University
В рамках проекта создавался тканевый аортальный клапан с гибридной каркасной конструкцией. Подобный клапан может быть использован для восстановления работы сердца как замена полноценному аортальному клапану.
В качестве каркаса для клапана использовался стент, представляющий из себя трубчатую структуру из искусственных тканей. Трубка пришивается к стенту в трех точках. В результате незашитые области раскрываются и образуют трехстворчатый клапан. Тканевый каркас использовался для улучшения механических свойств клапана.

Экспериментальная модель искусственного аортального клапана
В проекте использовалась технология FSI для совместного моделирования течения крови и деформации створок клапана. С помощью совместного расчёта аэрогидродинамического и прочностного пакетов FlowVision - Abaqus был проведён двунаправленный FSI-анализ с учётом повышенной податливости конструкции и наличием зазора между контактными поверхностями.
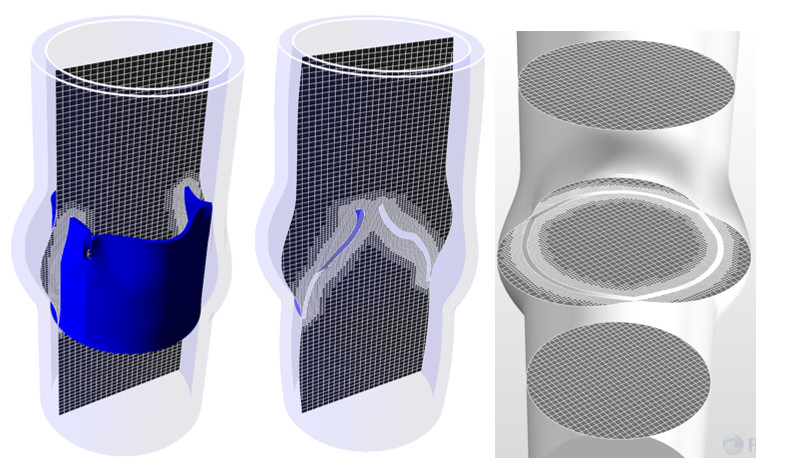
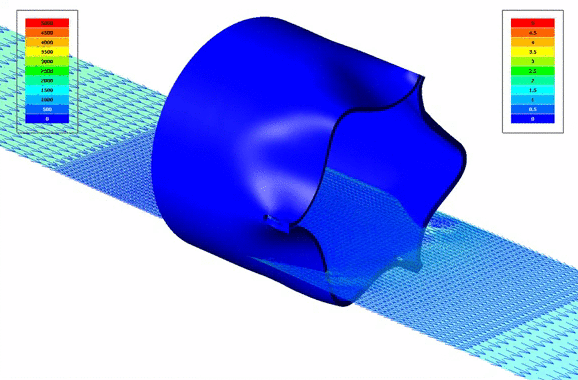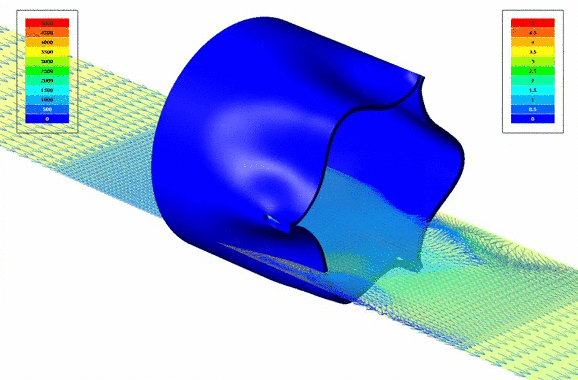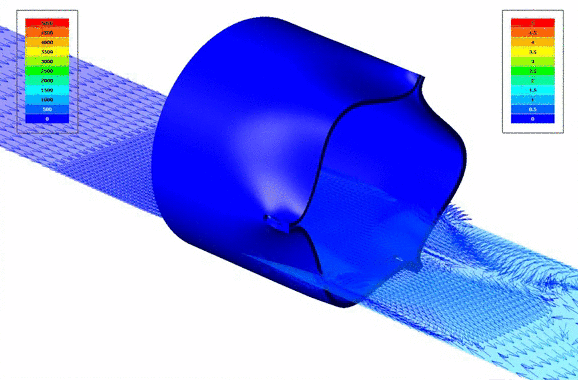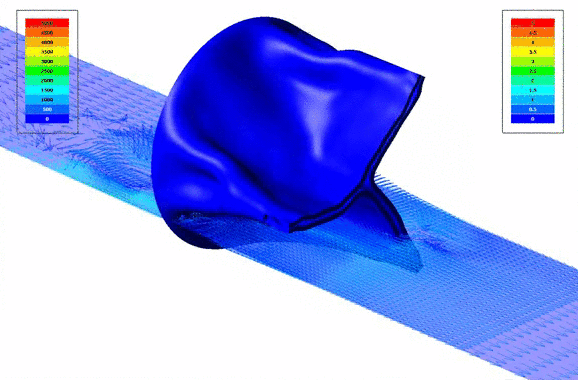 Визуализация векторов скоростей кровотока через клапан
Визуализация векторов скоростей кровотока через клапан
Сканирование сердца
при сотрудничестве с Charité – Universitätsmedizin Berlin
В рамках проекта проводилось исследование гемодинамики в живом сердце. Моделирование осуществлялось на геометрии, полученной путем сканирования реального сердца.
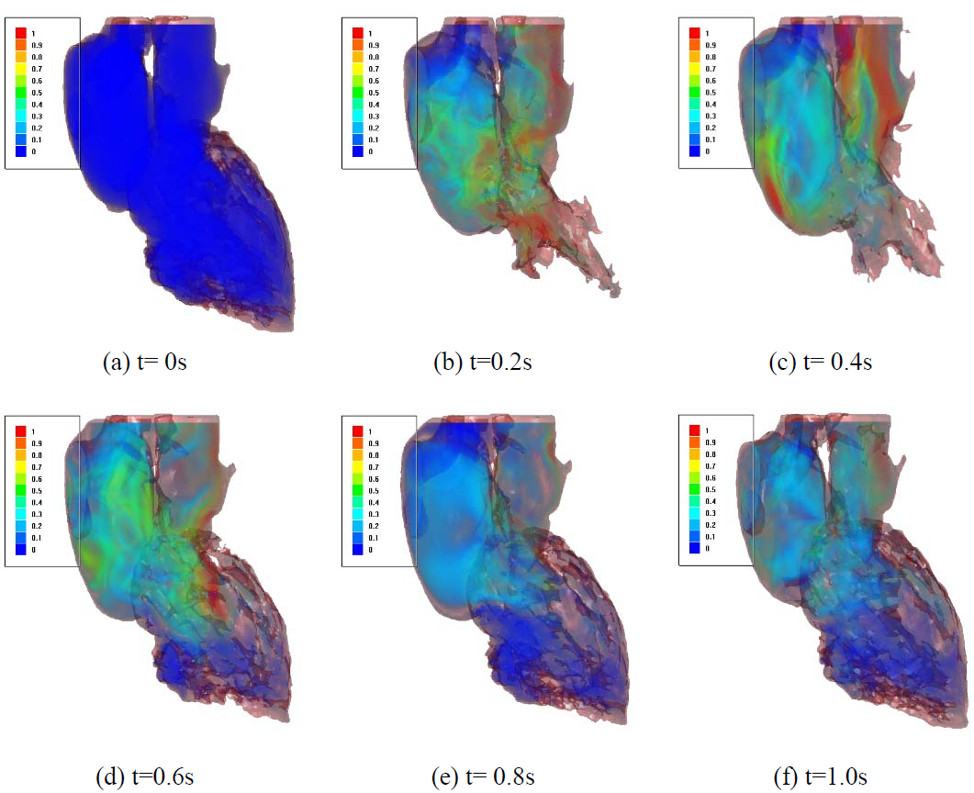
Для имитации процесса сердцебиения, при котором форма сердца изменяется со временем, с помощью магнитно-резонансной томографии было получено 100 кадров сердца. Полученные геометрии импортировались в программный комплекс вычислительной гидро- газодинамики FlowVision, где происходило моделирование внутреннего кровотока, и поверхности сердца автоматически заменялись через определенный интервал времени с сохранением промежуточного результата.
Численное моделирование позволило получить распределения скоростей и давлений кровотока в объеме бьющегося сердца.
Распределение скоростей в объеме сердца в разные моменты времени
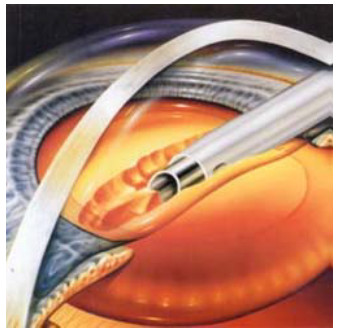
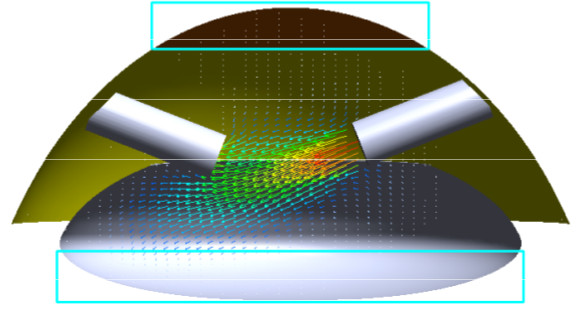
Моделирование промывки глаза при хирургии катаркты
Проект посвящен моделированию этапа промывки глаза в нескольких задачах: во время операции по лечению катаракты методом бимануальной факоэмульсификации (ФЭК) и по лечению катаракты методом коаксиальной ФЭК. В последней задаче рассмотрен также случай с имплантированной ранее факичной интраокулярной линзой.
Целью предварительного численного моделирования было уменьшение вероятности травмирования глаза в центральной области роговицы путём оптимизации положений хирургических инструментов, сравнение полученных результатов для различных методик операции.
В результате были найдены оптимальные положения инструментов при бимануальной и коаксиальной ФЭК, при которых сила трения на центральной поверхности роговицы минимальна.
Моделирование операции по удалению катаракты:
Моделирование воздушного потока в трахее
Исследовалось осаждение частиц, вводимых в ротовую полость. Частицы оседают на стенке вследствие ударов и диффузии. Задача состояла в том, чтобы исследовать особенности в поведении осаждения частиц с разными характеристиками. Для решения задачи использовалась подробная биологически точная модель дыхательных путей от мягкого неба до диафрагмы.
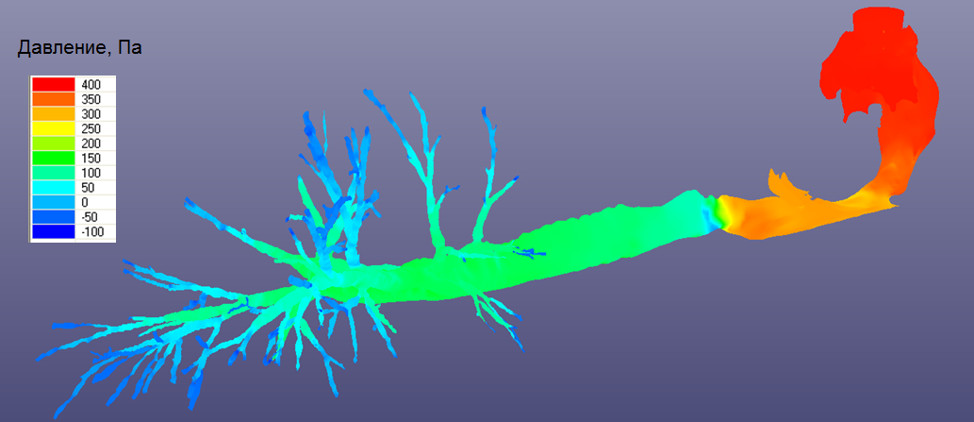
Результаты: распределение давления по поверхности трахеи